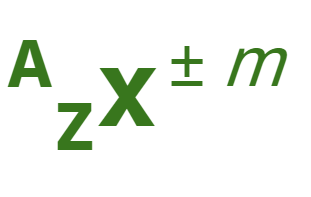
এখানে X দ্বারা কোন একটি মৌলের প্রতীক বােঝানাে হয়েছে। A দ্বারা বােঝানাে হয়েছে মৌলটির ভর সংখ্যা । Z দ্বারা মৌলটির পারমাণবিক সংখ্যা অর্থাৎ প্রােটন সংখ্যা বােঝানাে হয়েছে । +– m দ্বারা মৌলটি কয়টি ইলেকট্রন ত্যাগ বা গ্রহণ করেছে তা বােঝানাে হয়েছে। যদি মৌলটি ইলেকট্রন গ্রহণ করে তবে (- m) হয়, আর যদি মৌলটি ইলেকট্রন ত্যাগ করে তবে (+ m) হয়। আর মৌলটি যদি ইলেকট্রন গ্রহণ বা ত্যাগ কিছুই না করলে m = 0 হয়। এখান থেকে মৌলের নিউট্রন সংখ্যা(A-Z) , মৌলের ভর সংখ্যা (A), মৌলের পারমাণবিক সংখ্যা (Z) ইত্যাদি বের করা যায়। এখানে X = মৌলের প্রতীক। Z= মৌলের পারমাণবিক সংখ্যা। এটি প্রতীকের বাম পার্শ্বে পাদবিন্দুতে বসে। A = পরমাণুর ভর সংখ্যা। এটি প্রতীকের বাম পার্শ্বে শীর্ষবিন্দুতে বসে। এটি প্রােটন ও নিউট্রনের মােট সংখ্যা। একে নিউক্লিয়ন সংখ্যাও বলা হয়। +– m= আধানের পরিমাণ। এটি প্রতীকের ডান পার্শ্বে শীর্ষবিন্দুতে বসে। সংখ্যা লিখে তারপর চিহ্ন দিতে হয়।